免疫检查点阻断(ICB)的肿瘤免疫疗法已经取得了显著的临床进展。然而,由于结直肠癌的肿瘤突变负荷低和新生抗原的缺乏,存在患者响应率低等问题,亟需探索可介导肿瘤免疫治疗响应由“冷”变“热”的新策略。近日,我校交叉科学研究院栾鑫研究员和陈红专教授团队在医学1区杂志Theranostics上发表最新研究成果,成功设计构建抗PD-L1多肽偶联构象锁定蜂毒肽MP9的多肽嵌合物(PEG-MP9-aPDL1),借助抗PD-L1多肽和PEG化修饰,实现蜂毒溶瘤肽的肿瘤组织特异性靶向,高效裂解肿瘤细胞膜诱导肿瘤细胞免疫原性死亡,并进一步协同抗PD-L1多肽实现增强的结直肠癌溶瘤免疫疗效。

天然蜂毒溶瘤肽具有结构简单、合成简便、潜在风险低等特点,能“以毒攻毒”快速裂解肿瘤细胞膜,释放肿瘤特异性抗原,有望联合免疫检查点抑制剂实现增强的抗肿瘤免疫效应。课题组前期发现蜂毒溶瘤肽普遍存在半衰期短、体内靶向性差等问题,采用构象锁定技术成功实现对天然蜂毒肽Mastoparan的结构设计改造,发现具有显著增强的α-螺旋刚性结构和溶瘤活性的全新先导分子MP9。在此基础上,进一步构建具有特异性靶向肿瘤组织的抗PD-L1多肽偶联蜂毒溶瘤肽MP9的多肽嵌合物(PEG-MP9-aPDL1),该嵌合物包含4个模块:四臂PEG、蜂毒溶瘤肽MP9、肿瘤微环境响应性MMP-2酶切linker及D型抗PD-L1靶向肽。该嵌合物可克服MP9的直接静脉给药带来的溶血副作用,并借助抗PD-L1的靶向作用实现肿瘤组织高分布,PEG-MP9-aPDL1可被肿瘤微环境中高表达的MMP-2切割,发挥高效溶瘤和免疫检查点封闭的协同治疗效果。
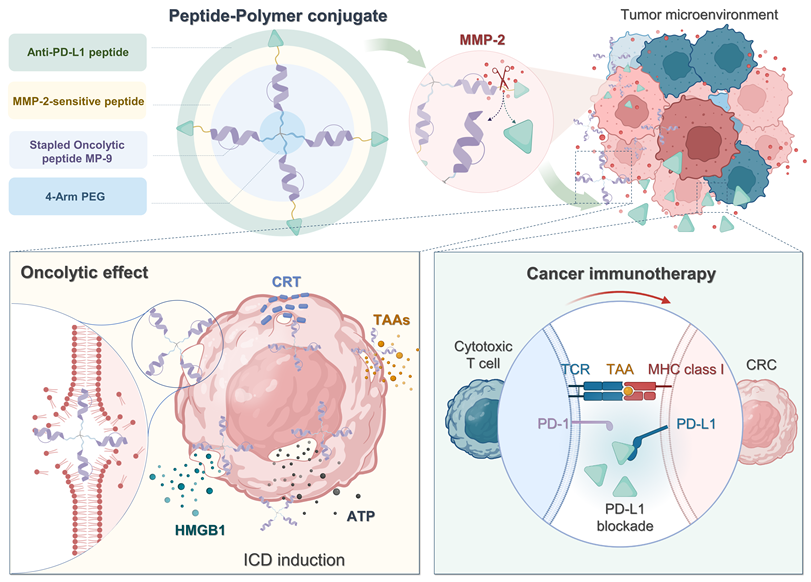
该研究中构建的“All in one”多肽嵌合物PEG-MP9-aPDL1成功实现蜂毒溶瘤肽和ICB治疗的高效协同,巧妙利用抗PD-L1多肽的肿瘤靶向和免疫检查点封闭的双重作用,有效克服现有溶瘤肽药物仅能瘤内注射的应用局限。研究为探索联合治疗改善结直肠癌免疫治疗响应,实现溶瘤肽类药物创新应用及靶向递送提供了重要科学思路和前期数据。
我校交叉科学研究院中药系统药理学研究中心栾鑫研究员、陈红专教授和吴也博士为论文的共同通讯作者,硕士研究生卢露、张鹤及密西西比大学Dr. Yu-Dong Zhou为论文的并列第一作者。该研究受到上海中医药大学交叉科学研究院张卫东教授和客座教授美国密西西比大学Prof. Dale G. Nagle的指导和大力支持。项目受到国家自然科学基金,国家中管局多学科交叉创新团队,上海市中药化学生物学前沿基地等多个项目的资助和支持。(交叉科学研究院、科技处)

