近日,我校交叉科学研究院刘三宏研究员团队联合海军军医大学张卫东团队和北京中医药大学林生团队,在国际知名学术期刊Signal Transduction and Targeted Therapy (STTT)上发表了题为“Acevaltrate as a novel ferroptosis inducer with dual targets of PCBP1/2 and GPX4 in colorectal cancer”的最新研究成果。该研究首次报道了中药小分子乙酰缬草三酯(ACE)通过同时靶向铁伴侣蛋白PCBP1/2和关键抗氧化酶GPX4,高效诱导结直肠癌细胞发生铁死亡的作用机制。

铁死亡是一种由亚铁离子(Fe²⁺)依赖的脂质过氧化物过度累积引发的新型细胞死亡方式,已成为肿瘤治疗研究的热点。然而,单一的靶向策略(如仅抑制GPX4)常因肿瘤细胞复杂的抗氧化系统和代谢调控而效果有限,且传统化疗药物面临的耐药性、复发和转移问题依然严峻。
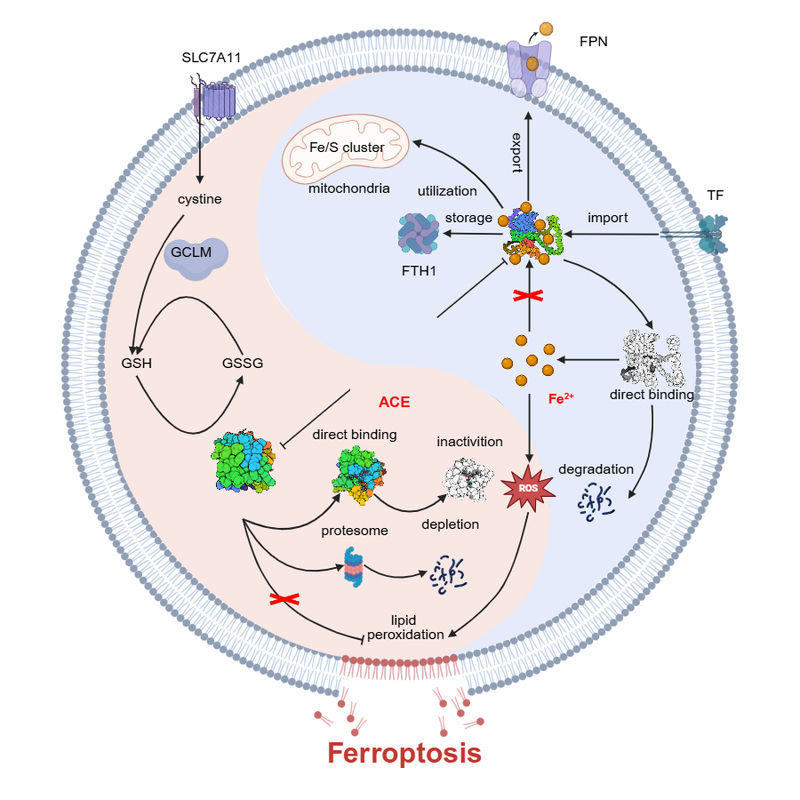
研究创新性地从天然产物库中筛选出ACE,并首次阐明其通过“双管齐下”的机制诱导结直肠癌细胞铁死亡:一方面,ACE直接结合并下调铁伴侣蛋白PCBP1和PCBP2的表达,导致细胞内游离Fe²⁺水平迅速升高;另一方面,ACE直接靶向结合GPX4蛋白的关键活性位点硒代半胱氨酸(U46),抑制其酶活性,并促进其通过泛素-蛋白酶体途径降解。这种同时破坏细胞内铁稳态和核心抗氧化防御系统的双重打击,使得ACE诱导铁死亡能有效克服抗氧化系统代偿和奥沙利铂耐药。更为重要的是,动物实验表明,口服ACE能显著抑制结直肠癌小鼠移植瘤的生长,其效果优于临床一线药物卡培他滨和TAS-102,也优于已知的铁死亡诱导剂索拉非尼和青蒿素。在治疗剂量下,ACE未表现出明显的肝肾毒性或引起正常组织亚铁离子异常积累。此外,在结直肠癌患者来源的类器官模型中,ACE表现出极高的敏感性(IC50值58-340 nM),进一步凸显了其临床应用潜力。这些发现为开发基于诱导铁死亡的新肿瘤治疗策略提供了科学依据,并且对ACE临床前研究奠定了基础,为结直肠癌等肿瘤的治疗提供了新的策略和希望。
我校交叉科学研究院博士研究生于典平、胡洪梅、张清和上海实验动物研究中心王成稷为论文共同第一作者。我校刘三宏研究员、海军军医大学张卫东教授、我校王群副研究员和北京中医药大学林生研究员为论文共同通讯作者。研究得到国家重点研发计划、国家自然科学基金、国家中医药管理局创新团队项目、上海市中药化学生物学前沿研究基地项目等资助支持。(科技处、交叉科学研究院)

