近日,我校交叉科学研究院葛广波讲席教授、郭兆彬青年研究员团队与澳大利亚阿德莱德大学Chih-Tsung Yang研究员团队合作,在国际权威期刊、自然指数期刊Advanced Functional Materials发表题为《A Vascularized Lung Tumoroid-on-a-Chip Model for the Accurate Assessment of Anti-Invasion Agents》的研究论文。该研究成功构建了一种新型血管化肺癌类器官芯片,其不仅可实现肿瘤-血管相互作用的动态可视化,还可通过精准量化肿瘤-血管嵌合体形成等肿瘤转移关键事件,筛选和评价抗非小细胞肺癌转移药物的药效。

非小细胞肺癌(NSCLC)患者的5年生存率仅为5%,而肿瘤转移是导致患者死亡的主要原因。血管是NSCLC转移的主要通道,阻断肿瘤细胞通过血管系统实现转移是抑制NSCLC转移的重要策略。然而,目前常用的肺癌体外模型普遍缺乏具备高仿生特性的血管结构,难以真实模拟肿瘤与血管之间的相互作用,也无法动态再现肿瘤转移的关键过程,这严重制约了抗转移药物疗效的精准评估。针对上述瓶颈,我校交叉科学研究院葛广波、郭兆彬团队借助微流控芯片等前沿技术,构建了一种新型血管-肺癌类器官芯片(Vascularized Lung Tomoroid-on-Chip, VLTOC),其可高仿生模拟肿瘤-血管嵌合体的形成、EPR效应等肿瘤转移关键事件。进一步借助荧光成像、超高分辨成像等技术对上述关键事件进行单细胞分辨率的原位实时追踪。组学分析显示VLTOC中肿瘤细胞增殖、代谢、侵袭及血管生成相关通路显著上调,较传统3D肿瘤球更贴近恶性进展表型,并揭示了细胞骨架动态重塑是驱动肺癌血管嵌合体形成的关键因素。
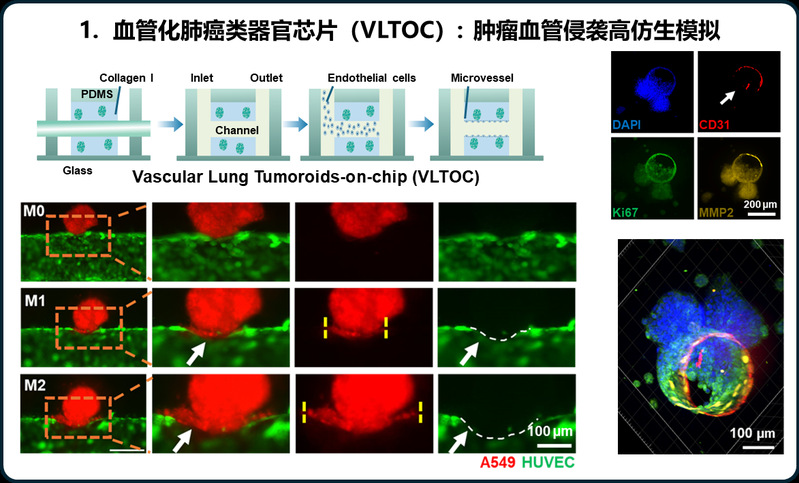
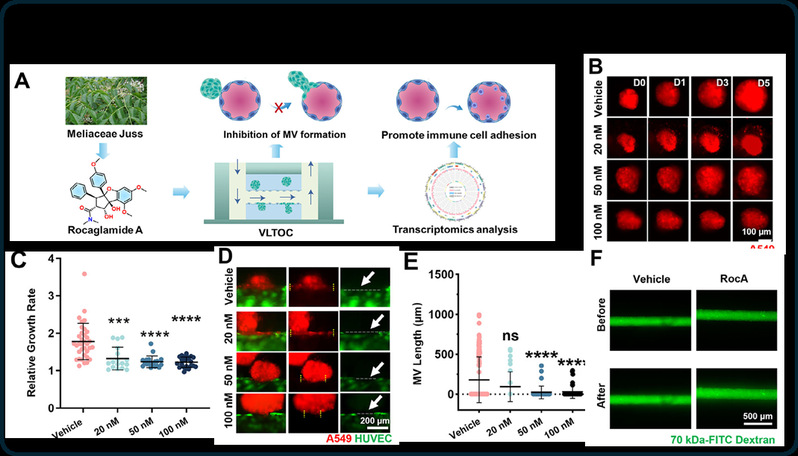
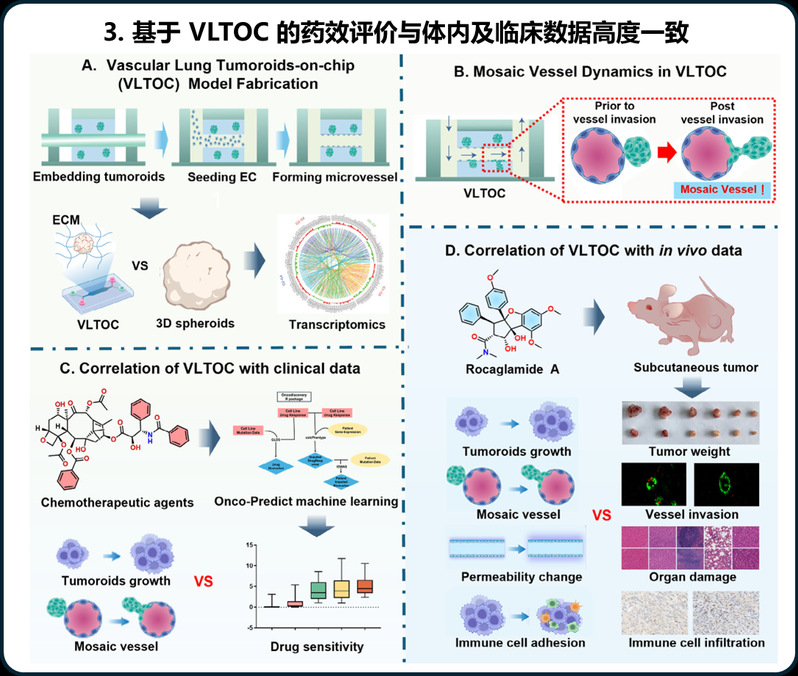
基于VLTOC模型,研究团队构建了同步表征肿瘤生长、血管嵌合体动力学及健康血管损伤的多参数药效评价体系。借助该体系对临床常用化疗药物的抗肺癌转移能力进行评价,发现嵌合血管扩张抑制率与TCGA患者数据库来源的药物敏感性预测结果高度相关,且显著优于肿瘤生长抑制等经典指标。在此基础上,研究团队还开展了中药活性成分楝酰胺的抗肺癌转移能力研究,发现该化合物在芯片中呈现抑制嵌合血管、保护血管完整性、促进免疫细胞粘附的三重药效特征。进一步的动物实验证实VLTOC平台可用于新型抗NSCLC迁移药物的疗效评估与脱靶毒性预警。
未来,研究团队将进一步提高模型仿生能力,并结合多种可视化药理学策略,有望在单细胞水平解析肿瘤侵袭、血管重构及免疫细胞归巢的动态过程,为揭示转移机制与筛选靶向干预分子提供可视化研究工具,推动该类器官芯片在抗肿瘤药物临床前评价、机制研究及临床精准用药等领域中的应用。
我校交叉科学研究院硕士研究生王学瑞和澳大利亚阿德莱德大学Guang Zhu博士为该论文的共同第一作者。葛广波研究员、郭兆彬青年研究员和澳大利亚阿德莱德大学研究员Chih-Tsung Yang博士为该论文的共同通讯作者,上海中医药大学为该论文第一通讯单位。澳大利亚阿德莱德大学Benjamin Thierry教授团队和上海市中医医院肿瘤临床医学中心主任田建辉教授团队为该研究提供了技术支持。该研究工作得到国家自然科学基金、国家重点研发计划、上海市伙伴科研计划等项目的支持。(科技处、交叉科学研究院)

