交叉科学研究院葛广波团队研发新型hCES2A共价抑制剂用于缓解伊立替康诱导的肠毒性
近日,我校交叉科学研究院葛广波团队在国际学术期刊《Acta Pharmaceutica Sinica B》上在线发表题为“Discovery of orally active and serine-targeting covalent inhibitors against hCES2A for ameliorating irinotecan-triggered gut toxicity”的研究论文。该研究通过规模化筛选、基于结构的药物设计和成药性优化策略,成功研发了新型口服有效且靶向丝氨酸的人羧酸酯酶2A(hCES2A)共价抑制剂C3,该抑制剂口服后显现出了良好的安全性和肠道高暴露等特点,其可有效缓解伊立替康诱导的荷瘤小鼠肠道毒性。

hCES2A是一种在肠道中高表达的丝氨酸水解酶,参与多种酯类前体药物的代谢活化过程,包括抗肿瘤药物伊立替康(CPT-11)。CPT-11作为治疗多种实体瘤和转移性癌症的常用药物,需经肝脏羧酸酯酶(CES)代谢转化为活性代谢物SN-38,才能发挥疗效。然而,由于人类肝脏CES对CPT-11的转化效率较低,大量CPT-11会通过胆汁排泄进入肠道,并被肠道中的hCES2A水解活化为高毒性代谢产物SN-38,进而引发严重的迟发性腹泻和肠道炎症,极大地限制了CPT-11的临床应用。临床上目前采用洛哌丁胺缓解CPT-11的肠道毒性,其不仅疗效有限,还可能引发心律失常、药物依赖和中枢性阿片效应等不良反应。因此,有必要研发可靶向抑制肠道hCES2A的候选药物用于缓解CPT-11引发的肠道毒性(ITGT)。
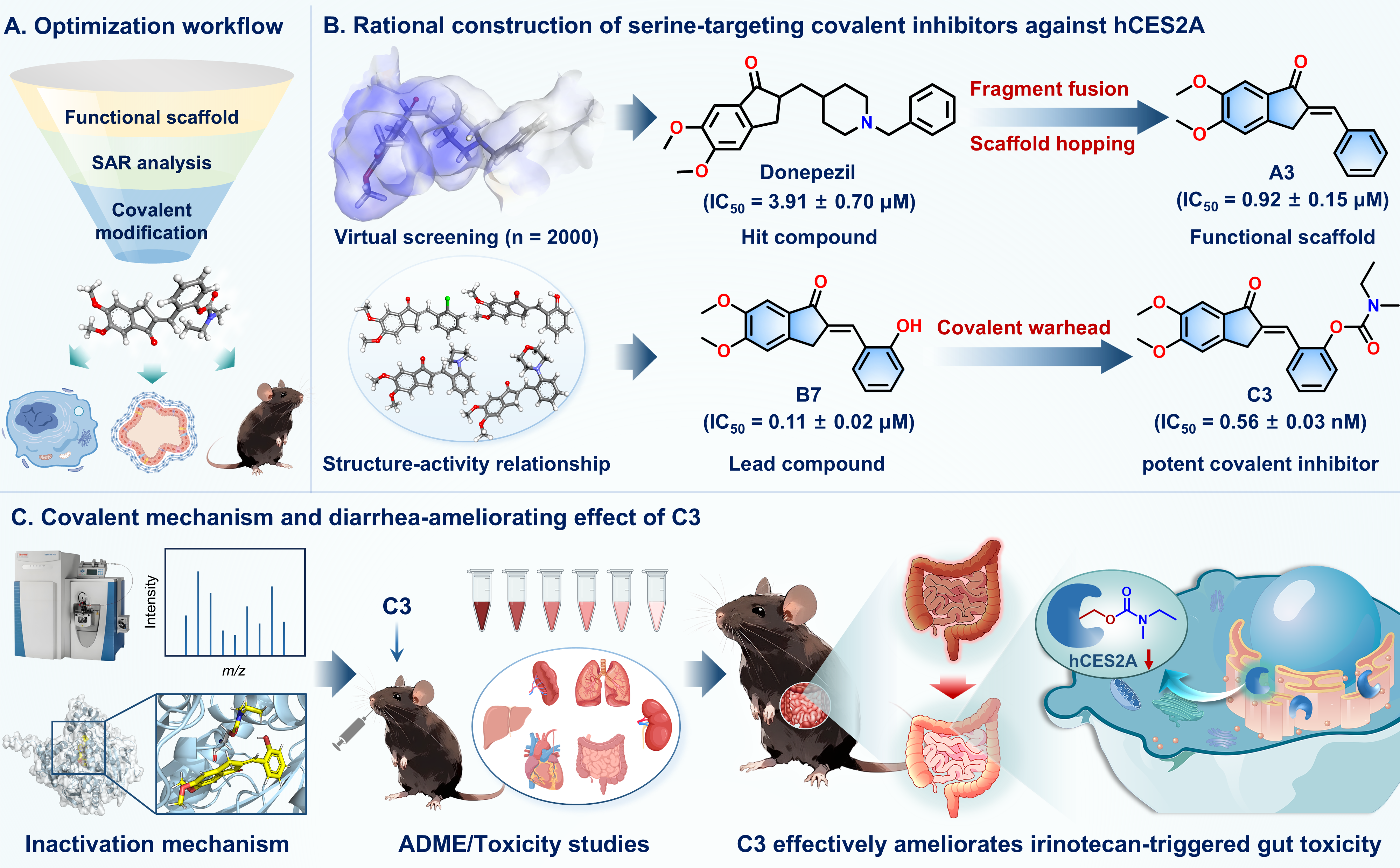
针对上述问题,研究团队采用基于结构的虚拟筛选和高通量酶抑制实验相结合的策略,从2000种FDA批准上市药物中筛选出了多奈哌齐(Donepezil)作为hCES2A的中等强度抑制剂(IC50 = 3.91 μM)。随后,利用片段融合、骨架跃迁、构效关系分析及共价靶头修饰等系列策略,成功研发出新型氨基甲酸酯类共价抑制剂C3(IC50=0.56 nM)。C3能够特异性共价修饰hCES2A催化空腔内的关键丝氨酸残基(Ser-228与Ser-236),并以时间和剂量依赖的方式强效抑制hCES2A活性。共价对接和分子动力学模拟进一步揭示:C3的氨基甲酸酯部分可使hCES2A催化口袋构象更趋紧凑,从而阻碍底物进入催化口袋。C3口服后展现出良好的安全性与高肠道暴露特性,其可在肠S9、活细胞、肠道类器官及荷瘤小鼠等多个生物维度中有效抑制hCES2A水解活性,从而显著缓解CPT-11引起的肠毒性。该研究不仅为改善CPT-11诱导的肠道毒性提供了极具潜力的候选药物,也为开发靶向丝氨酸水解酶的共价抑制剂提供了重要的研究范例。
相关工作已同步申请了国家发明专利。海南大学桑志培副教授与大连医科大学陈大朋教授分别在共价抑制剂合成与药效表征方面提供了大力支持。我校交叉科学研究院硕士研究生张雅、博士后范玉凡、实验师宋云清、博士研究生朱广灏为论文共同第一作者,葛广波讲席教授、桑志培副教授、陈大朋教授和曾海荣博士为论文共同通讯作者,上海中医药大学为论文第一单位和通讯单位。该研究工作得到国家重点研发计划和国家自然科学基金等项目的支持。(科技处、交叉科学研究院)
